相达生物获3400万美元融资,开发宫颈癌早筛新方式,HPV尿液检测离应用还有多远
5月20日,相达生物科技宣布完成3400万美元的A轮融资。最新融资由亚洲最大独立资产管理公司之一的惠理集团旗下私募基金领投,这笔融资也创下了2019年以来亚洲诊断技术领域最大规模的A轮融资。
图片来源于网络,如有侵权,请联系删除
此前,相达生物开发的全球首款人类乳头瘤病毒(HPV)尿液基因检测相关数据公布,为宫颈癌等疾病的早期筛查提供了新的可能性。
图片来源于网络,如有侵权,请联系删除
HPV检测技术近期在美国获得临床突破。上周,美国FDA批准了首个家用宫颈癌筛查检测试剂,该试剂由Teal Health公司开发。今年年初,Teal Health在最新一轮融资中筹集了1000万美元。
图片来源于网络,如有侵权,请联系删除
居家检测试剂能让宫颈癌筛查更容易通过远程医疗进行,并可在家自行进行取样,而无需前往诊所。
第一财经记者了解到,Teal Health采取的检测方式是阴道拭子,由女性自行在阴道内取样。尽管该产品为女性自行居家检测提供便捷,但这种方式仍然属于侵入式,而尿液检测的方式为非侵入式。
相达生物科技董事长及首席执行官招彦焘告诉第一财经记者,大多数人更愿意选择尿液检测。“调查显示80%的人偏好尿液方式。”他说道,“这种非侵入式的检测方式不仅适用于女性,也同样适用于男性HPV检测。”
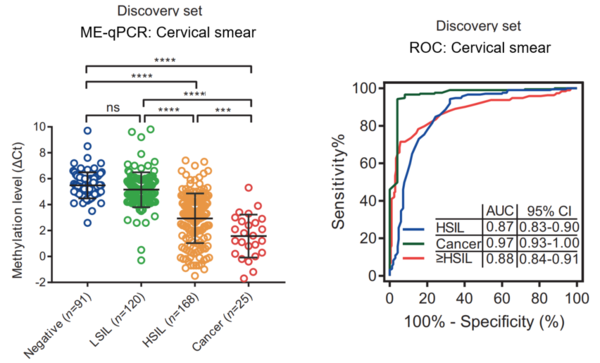
据相达生物此前公布的数据,在与北京大学深圳医院合作的最新临床研究中,该尿液检测对CIN2+病变(包括子宫颈癌前病变及子宫颈癌)的灵敏度达93.4%,并且在HPV 16型及18型的检测中,与医生采集样本的黄金标准检测(罗氏Cobas 4800)相比,达到超过97%的一致性。
目前,包括诺辉健康在内的多家检测公司也都在开发相关产品,但国内还没有任何HPV尿检产品或居家检测产品获批。招彦焘对第一财经记者表示,目前相达生物的检测产品在国内仍处于临床注册阶段,即将启动大规模临床试验。
“我们会在美国、中国和中国香港三地同步推动临床,并可通过LDT模式商业化。”招彦焘说,他预计产品从临床走向最终获批上市可能需要一年多时间。
在谈及这种尿液检测的成本时,招彦焘对第一财经记者说道,目前的成本与罗氏的金标准检测方法成本相当。“我们的目标是一年内可将成本降至与国内阴道拭子检测成本同等水平,从而使得最终售价与传统采样方式接近,并有一定的利润空间。”他表示。
HPV感染是宫颈癌的风险因素。但目前女性宫颈癌早期筛查仍存在巨大的空白。根据国家卫健委2023年发布的《关于印发加速消除宫颈癌行动计划(2023-2030)的通知》,到2025年,适龄妇女宫颈癌筛查率达到50%;到2030年,适龄妇女宫颈癌筛查率达到70%,与世界卫生组织提出的目标一致。
招彦焘认为,传统的HPV检测方式限制了一部分女性主动前往医疗机构进行筛查的意愿,未来尿液检测相关产品如能上市,将进一步填补女性宫颈癌早筛市场未被满足的需求,并开辟目前几乎为空白的男性HPV检测市场。
